Gruppe 3
PH bei Lungenerkrankungen und/oder Hypoxie
Definition
Die pulmonale Hypertonie (PH) assoziiert mit Lungenerkrankungen und/oder Hypoxie bildet die PH-Gruppe 3 gemäß WHO- und Nizza-Klassifikation.1
Zu dieser Gruppe zählen eine (häufig beobachtete) PH infolge einer chronisch obstruktiven Lungenkrankheit (COPD) und/oder einem Emphysem, interstitiellen Lungenerkrankungen (ILD), einer Mischform von Lungenfibrose und -emphysem (CPFE) und Hypoventilationssyndromen.1–3 Weiterhin umfasst die PH-Gruppe 3 eine PH assoziiert mit einer obstruktiven Schlafapnoe – diese tritt selten auf, außer andere Grundbeschwerden wie COPD oder Hypoventilationssyndrome am Tage (z. B. bei Adipositas) liegen vor.1,4 Für Höhenbewohner (ab 2.500 Meter über dem Meeresspiegel) hingegen gilt ein erhöhtes Risiko für eine Hypoxie-induzierte PH.1,4
Hämodynamische Definition der PH-Gruppe 3 (präkapilläre PH):1 | |
|---|---|
Mittlerer Pulmonalarteriendruck (mPAP) | > 20 mmHg |
Pulmonalarterienverschlussdruck (PAWP) | ≤ 15 mmHg |
Pulmonalvaskulärer Widerstand (PVR) | > 2 WU |
Klassifikation
Die PH-Gruppe 3 infolge von Lungenerkrankungen und/oder Hypoxie ist auf eine Vielzahl an Ursachen und eine komplexe Pathophysiologie zurückzuführen.1,4 Darunter fallen auch eine nicht diagnostizierte CTEPH oder PAH sowie kardiale Komorbiditäten bei einer Lungenerkrankung, die zu einer PH führen können.1
Die WHO-Klassifikation unterteilt die Gruppe nach ihrer Ätiologie in folgende Unterformen:1,2
Obstruktive Lungenerkrankung oder Emphysem
Restriktive Lungenerkrankung
Andere Lungenerkrankung mit gemischt restriktivem/obstruktivem Muster
Hypoventilationssyndrome
Hypoxie ohne Lungenerkrankung
Entwicklungsbedingte Lungenerkrankungen
Epidemiologie und Risikofaktoren
Die PH infolge von Lungenerkrankungen und/oder Hypoxie kommt häufig vor:1
1–5 % der Fälle mit fortgeschrittener COPD mit chronischer Luftnot oder Kandidatinnen und Kandidaten für Lungenvolumenreduktions-OP oder Lungentransplantation haben einen mPAP > 35–40 mmHg.1
8–15 % der Fälle von idiopathischer Lungenfibrose bei Erstuntersuchung, 30–50 % im fortgeschrittenen Stadium und > 60 % im Endstadium haben einen mPAP ≥ 25 mmHg.1
47–90 % der an CPFE-Erkrankte entwickeln eine schwere PH.3
5 % der Höhenbewohner (> 2.500 Höhenmeter) erkranken an einer PH aufgrund geographischer und genetischer Faktoren (gesamt ca. 120 Mio. Betroffene).1,4
Zu den Risikofaktoren gehören ein höheres Alter (in einer Studie mit n = 434 lag das mediane Alter bei 72 Jahren), männliches Geschlecht und Rauchen.1,5
Klinische Charakterisierung, Schweregrad und Prognose
Das klinische Bild überschneidet sich mit den Symptomen der zugrunde liegenden Lungenerkrankung, insbesondere der Belastungsdyspnoe.1 Die klinischen Manifestationen sind hauptsächlich unspezifisch, wie z.B. Knöchelödeme.1
Häufig tritt die PH-Gruppe 3 in nicht schwerwiegender Form auf (PVR ≤ 5 WU).1 Dennoch hat sie Einfluss auf die Morbidität und Mortalität.1
Die schwerwiegende Form (PVR > 5 WU) hingegen ist selten.1 Sie betrifft 1–5 % der COPD-Erkrankten und < 10 % der Fälle mit fortgeschrittener ILD.1 Die Prognose ist schlechter als bei nicht schwerwiegender Ausprägung, weshalb eine sofortige Überweisung an ein PH-Expertenzentrum notwendig ist.1
Eine PH infolge einer ILD geht mit einer eingeschränkten Lebensqualität und einer schlechter Prognose einher.3,4 Das Adipositas-Hypoventilationssyndrom (OHS) ist oftmals schwerwiegend und mit einer Rechtsherzinsuffizienz assoziiert.4
Den höchsten prädiktiven Wert für die Mortalität hat die Einteilung nach WHO-Funktionsklassen (WHO-FC).1
Class | Descriptiona |
|---|---|
WHO-FC I | Patients with PH but without resulting limitation of physical activity. Ordinary physical activity does not cause undue dyspnoea or fatigue, chest pain, or near syncope |
WHO-FC II | Patients with PH resulting in slight limitation of physical activity. They are comfortable at rest. Ordinary physical activity causes undue dyspnoea or fatigue, chest pain, or near syncope |
WHO-FC III | Patients with PH resulting in marked limitation of physical activity. They are comfortable at rest. Less than ordinary activity causes undue dyspnoea or fatigue, chest pain, or near syncope |
WHO-FC IV | Patients with PH with an inability to carry out any physical activity without symptoms. These patients manifest signs of right HF. Dyspnoea and/or fatigue may even be present at rest. Discomfort is increased by any physical activity |
PH, pulmonary hypertension; WHO-FC, World Health Organization functional class.
Tab. 1: WHO-Funktionsklasse (WHO-FC) der pulmonalen Hypertonie (PH). aFunktionelle Klassifizierung der PH, modifiziert nach der New York Heart Association (NYHA) gemäß WHO 1998. Modifiziert nach 1.
Diagnostik
Den diagnostischen Algorithmus beim Verdacht auf eine PH finden Sie hier.
Diagnostik
Echokardiographie: Nicht invasives Verfahren zur Diagnose der PH, bei fortgeschrittener Lungenerkrankung nicht zuverlässig.1–3 → für Parameter bitte hier klicken
Lungenfunktionstests (PFT) und arterielle Blutgasanalyse (ABG) inklusive Bestimmung der Diffusionskapazität (DLCO).1 Häufig liegt eine sehr niedrige DLCO vor (< 45 %).1
Elektrokardiogramm (EKG): Abweichungen im EKG können auf eine PH hinweisen.1 → für Parameter bitte hier klicken
Röntgenthoraxaufnahme und Computertomographie (CT): Bildgebende Verfahren können Anzeichen einer parenchymalen Lungenerkrankung zeigen.1 → für Parameter bitte hier klicken
Rechtsherzkatheter (RHC): Goldstandard für die PH-Diagnose und Klassifizierung.1–4,6 Bei PH-Gruppe 3 wird RHC eingesetzt, um die Notwendigkeit einer chirurgischen Behandlung zu evaluieren.1 Idealerweise findet die Durchführung bei klinisch stabilem Zustand unter optimierter Therapie der Grunderkrankung im PH-Expertenzentrum statt.1 → für Parameter bitte hier klicken
Weitere Untersuchungen: Sechs-Minuten-Gehtest, hämatologische, immunologische sowie Biomarker-Tests (BNP/NT-pro-BNP).1
Zu den wichtigsten Aspekten der Bewertung einer vermuteten PH-Gruppe 3 bei Lungenerkrankungen gehören:1
Bewertung klinischer Merkmale, u. a. Krankheitsverlauf, Sauerstoffbedarf
PFT inklusive DLCO und ABG
Nicht invasive Tests: BNP/NT-proBNP, EKG, Echokardiographie
Bildgebung: CT, SPECT oder V/Q-Lungenscan, ggf. Kombination aus Echokardiographie und kontrastverstärkte CT, ggf. cMRI
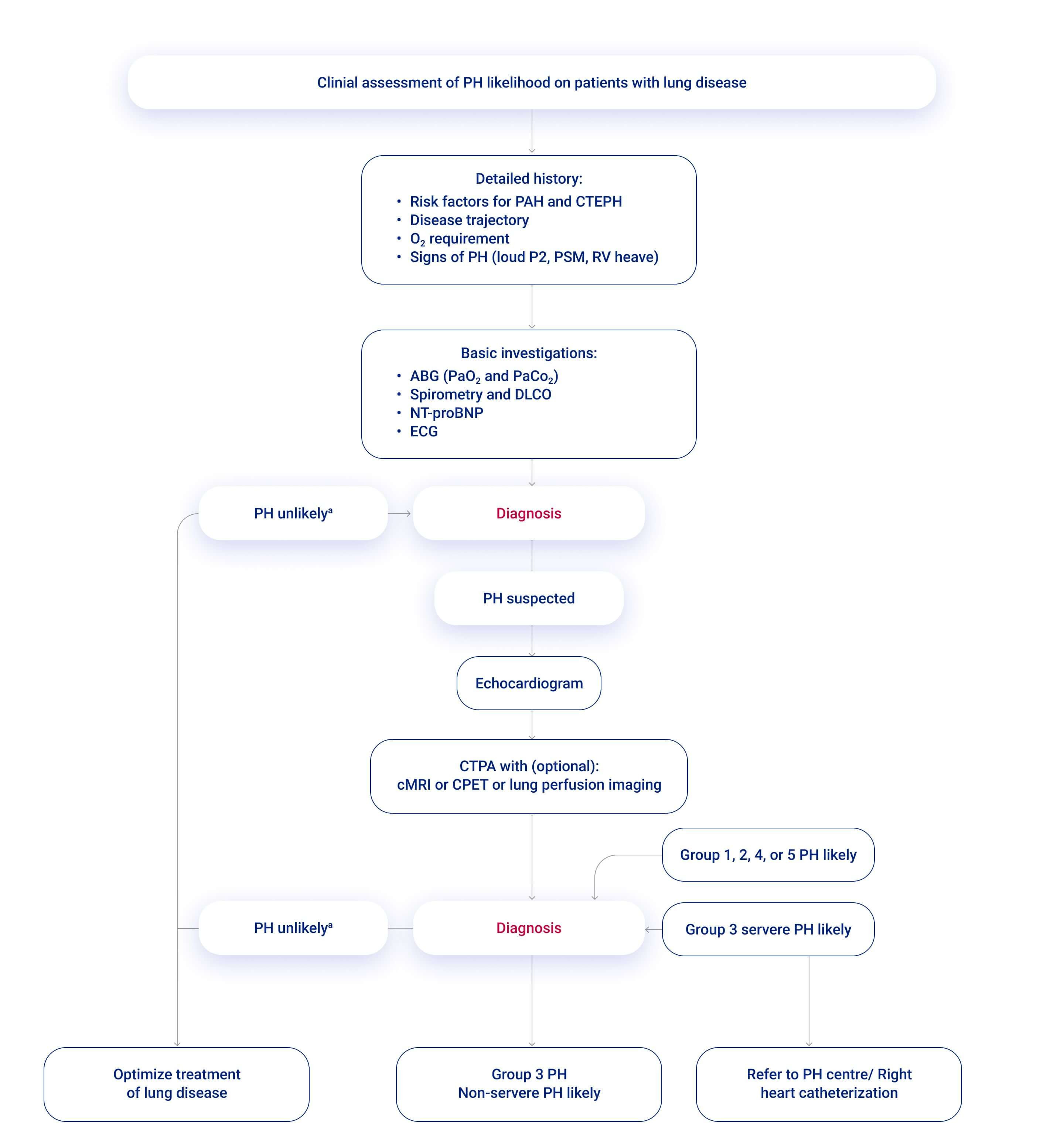
Abb. 1: Klinische Untersuchungen zur Wahrscheinlichkeit einer PH bei Lungenerkrankungen.a Untersuchungen müssen schrittweise in den klinischen Kontext integriert werden, um die Wahrscheinlichkeit und Ätiologie von PH zu ermitteln. Modifiziert nach 6.
Weiterführende Informationen zur Diagnostik finden Sie hier. Eine ausführliche Beschreibung in den aktuellen ESC/ERS-Leitlinien (2022) zur PH.1
Therapie
Der Fokus in der Behandlung der PH-Gruppe 3 liegt darin, die zugrunde liegende Lungenerkrankung zu optimieren, unter anderem durch:1
Sauerstofftherapie
Nicht invasive Beatmung
Aufnahme in Lungenrehabilitationsprogramme
Patientinnen und Patienten mit (vermuteter) schwerer PH und/oder schwerer RV-Dysfunktion oder bei Unsicherheiten bezüglich der Therapie sollten in ein akkreditiertes PH-Expertenzentrum zur individuellen Therapieentscheidung mit ggf. Einschluss in eine klinische Studie überwiesen werden.1
Bei geeigneten Erkrankten sollte eine Lungentransplantation in Betracht gezogen werden.1
Die klassischen für die PAH zugelassenen Arzneimittel sind nicht für die PH-Gruppe 3 indiziert.1,3,4 Die bisherigen Erfahrungen mit diesen Arzneimitteln bei der PH-Gruppe 3 sind begrenzt und widersprüchlich.1 Teilweise wurden negative Effekte auf Hämodynamik, Leistungskapazität und Gasaustausch beschrieben:1,3,4
Schwere PH assoziiert mit COPD oder Emphysem: erste Hinweise auf Verbesserung durch Sildenafil (PDE5i), aber aufgrund geringer Daten keine generelle Empfehlung.
PH infolge einer ILD: Eine randomisierte klinische Studie wies positive Ergebnisse unter inhalativem Treprostinil (PCA) nach; klinische Studien mit ERAs und PDE5i (Sildenafil) zeigten negative Resultate; unter Ambrisentan (ERA) und Riociguat (sGC) wurden schwerwiegende Effekte auf die Krankheitsprogression beobachtet.
Schwere (vermutete) PH mit COPD oder ILD: Überweisung an PH-Expertenzentrum zur Erwägung einer PAH-spezifischen Therapie auf individueller Basis.
Eine ausführliche Beschreibung der therapeutischen Strategie ist in den aktuellen ESC/ERS-Leitlinien (2022) zur PH zu finden.1
Verdacht auf PH ?
Bei Verdacht auf PH bei mit Lungenerkrankungen und/oder Hypoxie kontaktieren Sie hier unsere PH-Experten, um sich auszutauschen oder ein PH-Expertenzentrum in der Nähe.

ABG: Arterielle Blutgasanalyse
BNP/NT-proBNP: Brain natriuretic peptide/ N-terminales pro-BNP
cMRI: Kardiale Magnetresonanztomographie
COPD: Chronisch obstruktive Lungenkrankheit
CPET: Kardiopulmonale Belastungstests
CPFE: Kombinierte Lungenfibrose und Emphysem
CT: Computertomographie
CTEPH: Chronisch thromboembolische pulmonale Hypertonie
CTPA: Computertomographie, Lungenangiographie
DLCO: Kohlenmonoxid-Diffusionskapazität
EKG: Elektrokardiogramm
ERS: European Respiratory Society
ESC: European Society of Cardiology
ILD: Interstitielle Lungenerkrankung
mPAP: Mittlerer Pulmonalarteriendruck
P2: Zweiter Herzton
PaCO2: Partialdruck des arteriellen Kohlendioxids
PAH: Pulmonale arterielle Hypertonie
PaO2: Partialdruck des arteriellen Sauerstoffs
PAWP: Pulmonalarterienverschlussdruck
PFT: Lungenfunktionstest
PH: Pulmonale Hypertonie
PSM: Pansystolisches Geräusch
PVR: Pulmonalvaskulärer Widerstand
RV: Rechtsventrikulär
SPECT: Single-Photon-Emissionscomputertomographie
VQ-Scan: Lungenbeatmungs- /Perfusionsscan, Lungenszintigraphie
WHO: World Health Organization
Humbert M et al. Eur Heart J 2022; 43(38): 3818–3731.
DGPK, S2k-Leitlinie Pulmonale Hypertonie, Version 3.0, Stand 29.04.2020, verfügbar unter: https://register.awmf.org/de/leitlinien/detail/023-038 (letzter Zugriff am 08.04.2024).
Waxman AB et al. Eur Respir Rev 2022; 31(165): 210220.
Nathan SD et al. Eur Respir J 2019; 53(1): 1801914.
Hoeper MM et al. J Heart Lung Transpl 2020; 39: 1435–1444.
Humbert M et al. Eur Heart J 2022; 00, 1–112.