Allgemein
Pulmonale Hypertonie
Hürden der Diagnosestellung: pulmonale Hypertonie
Die Zeit von Symptombeginn bis zur Diagnosestellung bei pulmonaler Hypertonie (PH) beträgt häufig über 2 Jahre.1 Daher befinden sich viele der Patientinnen und Patienten, die zur (weiteren) Abklärung einem PH-Expertenzentrum zugewiesen werden, bereits in einem fortgeschrittenen Stadium, wurden fehldiagnostiziert oder erhalten eine inadäquate Therapie.2
Eine Dyspnoe selbst bei geringer Anstrengung kann auf eine pulmonale Hypertonie (PH) hinweisen.1,3 Die Diagnostik sollte, je nach Unterform, direkt im PH-Expertenzentrum erfolgen.1
Je früher die Diagnose gestellt wird, desto besser ist die Erkrankung behandelbar und desto günstiger ist die Prognose.1
Bedeutung der Expertenzentren für die Diagnosestellung
Häufig entsteht die lange Latenzzeit zwischen Erstvorstellung bis zur Diagnosestellung aufgrund einer Fehlinterpretation der Symptome.2 So wird z. B. eine, für die PH charakteristische, Dyspnoe für ein Symptom einer chronisch obstruktiven Lungenerkrankung (COPD) oder Asthma bronchiale gehalten.2
In einer Studie wurden 140 Patientinnen und Patienten, die sich erstmalig in einem PH-Expertenzentrum vorgestellt haben, untersucht.3,4
Die Ergebnisse zeigen, dass ein hoher Anteil der Patientinnen und Patienten fehldiagnostiziert, falsch klassifiziert und/oder nicht leitlinienkonform behandelt wurde:3,4
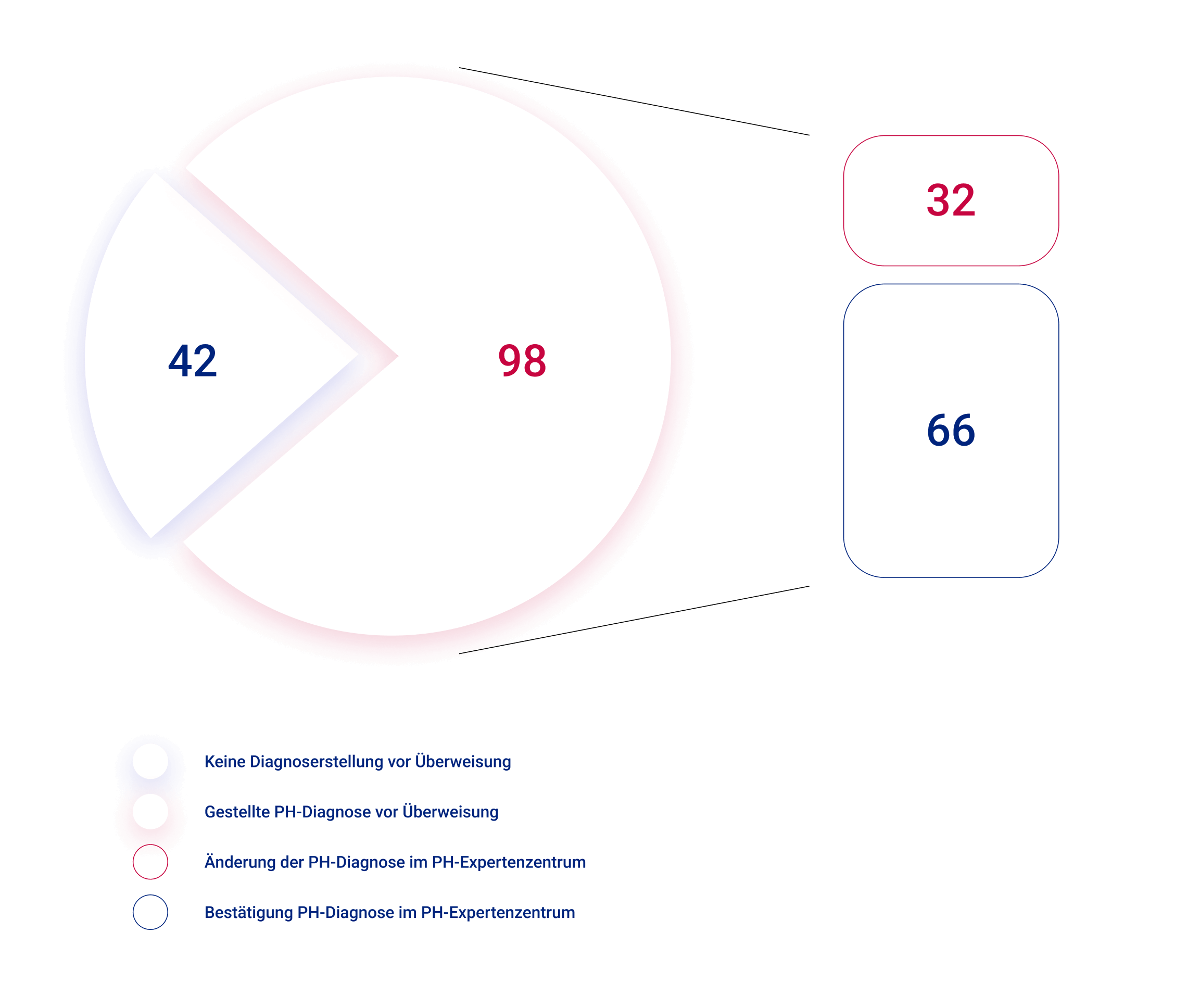
98 der Fälle wurden mit einer bereits gestellten PH-Diagnose überwiesen:
32 stellten sich dabei als fehldiagnostiziert heraus
66 Fälle wurden korrekt diagnostiziert; 42 davon erhielten eine PAH-spezifische Therapie vor Überweisung und 24 Fälle wurden nicht leitlinienkonform behandelt
Weniger als die Hälfte (42 der Teilnehmenden) wurden ohne vorherige Diagnosestellung in das PH-Expertenzentrum überwiesen
Die richtige Differentialdiagnose ist entscheidend für den Therapieerfolg
Für einige Untergruppen der PH gibt es wirksame Therapieoptionen, die bei anderen Formen wirkungslos sind oder sogar nachteilig sein können.1 Daher ist die exakte diagnostische Zuordnung bzw. die Differentialdiagnose der PH unerlässlich.1
Insbesondere bei Pulmoarterielle Hypertonie (PAH), Chronisch thromboembolische pulmonale Hypertonie (CTEPH) oder anderen schwerwiegenden Formen der PH ist eine frühzeitige Überweisung an ein PH-Expertenzentrum zur Diagnostik und Therapie erforderlich.1 Die CTEPH wird häufig als PAH fehldiagnostiziert und damit nicht leitliniengerecht behandelt.1
Vor allem bei PAH und CTEPH ist eine frühe Diagnose wichtig
PAH: Zwischen Symptombeginn und Diagnose vergehen im Mittel 2 oder mehr Jahre (Registerdaten aus den USA und Europa).5–9
CTEPH: Mittlere Latenzzeit 18 ± 26 Monate; in einer Studie ist diese Zeit bei Patientinnen und Patienten mit vorangegangenem Lungenembolie-Ereignis (n=56) 16,9 ± 23,8 Monate kürzer als bei solchen (n=13) ohne Lungenembolie (23,5 ± 36,9 Monate).10
Dabei tritt eine besondere Herausforderung auf: die PH-Formen zeigen sich selbst in den verschiedenen Altersgruppen (wie z. B. bei Neugeborenen, Kindern und Erwachsenen) sehr unterschiedlich:1
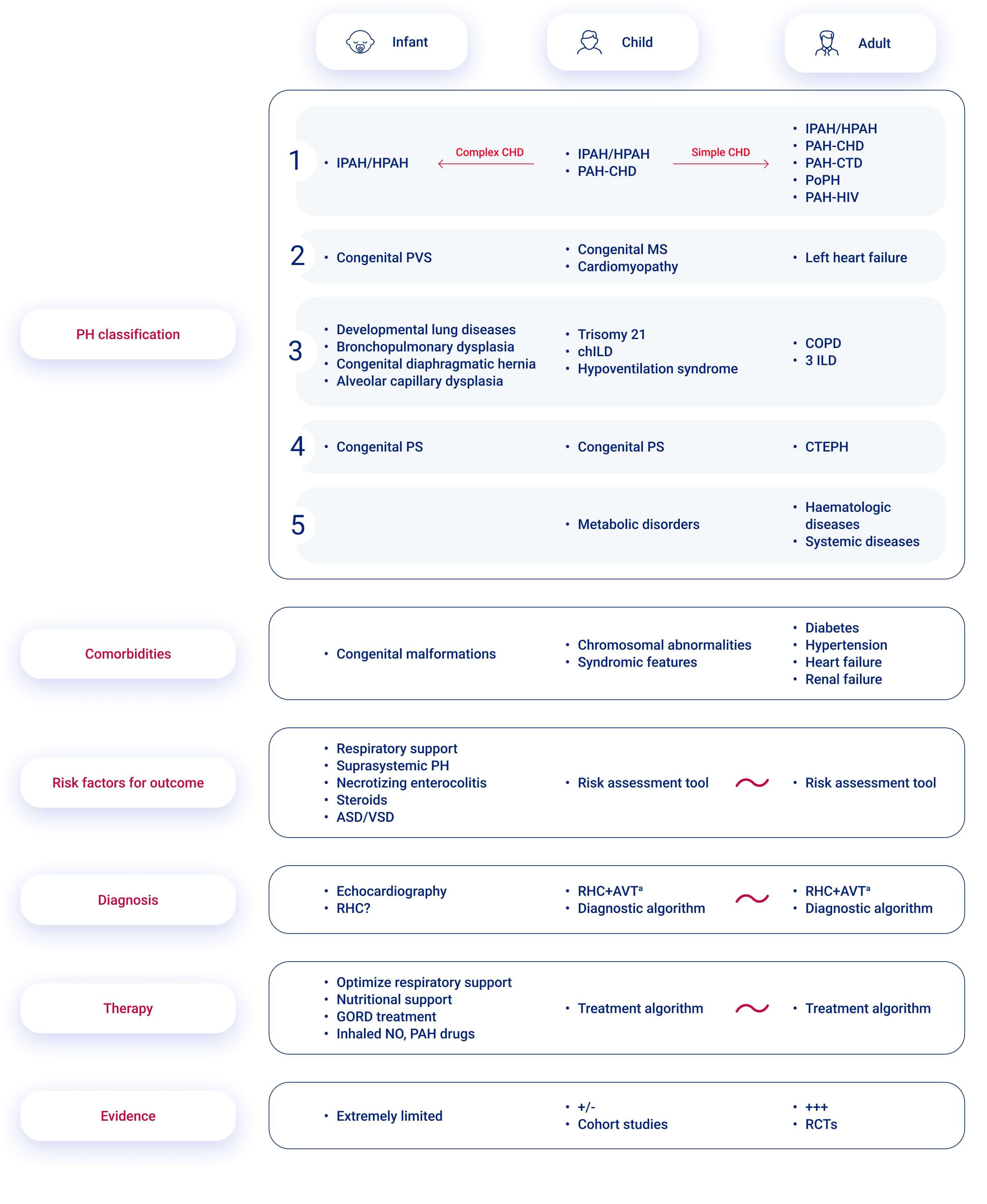
ASD, atrial septal defect; AVT, acute vasoreactivity testing; CHD, congenital heart disease; COPD, chronic obstructive pulmonary disease; CTEPH, chronic thrombo-embolic pulmonary hypertension; GORD, gastro-oesophageal reflux disease; HPAH, heritable pulmonary arterial hypertension; ILD, interstitial lung disease; IPAH, idiopathic pulmonary arterial hypertension; MS, mitral stenosis; NO, nitric oxide; PAH, pulmonary arterial hypertension; PAH-CHD, PAH associated with congenital heart disease; PAH-CTD, PAH associated with connective tissue disease; PAH-HIV, PAH associated with HIV infection; PH, pulmonary hypertension; PoPH, porto-pulmonary hypertension; PPHN, persistent pulmonary hypertension of the newborn; PS, pulmonary arterial stenosis; PVS, pulmonary vein stenosis; RCT, randomized controlled trial; RHC, right heart catheterization; VSD, ventricular septal defect. aIn patients with idiopathic, heritable or drug-associated PAH. Pulmonary hypertension in neonates and infants significantly differs in aetiology, pathophysiology, risk assessment, and treatment from older children and adults, while PH in older children has more similarities with PH in adults.
Außerdem müssen Grunderkrankung(en) und Komorbiditäten identifiziert werden, vor allem bei Linksherzerkrankungen (LHD, PH-Gruppe 2) und Lungenerkrankungen (PH-Gruppe 3).1 Die Klassifizierung, Risikobestimmung und – je Unterform – spezifische Behandlungen erfolgen im PH-Expertenzentrum.1
Definition: Pulmonale Hypertonie
Die PH wird definiert als Lungenhochdruck bei einem invasiv gemessenen pulmonalarteriellen Mitteldruck (mPAP) > 20 mmHg in Ruhe.1,2
Je nach Unterform unterscheiden sich die hämodynamischen Parameter:1
Definition | Haemodynamic characteristics |
|---|---|
PH | mPAP > 20 mmHg |
Pre Capillary PH | mPAP > 20 mmHg PAWP ≤ 15 mmHg PVR >2 WU |
IpcPH | mPAP > 20 mmHg PAWP ≤ 15 mmHg PVR ≤ 2 WU |
CpcPH | mPAP > 20 mmHg PAWP > 15 mmHg PVR > 2 WU |
Exercise PH | mPAP/CO slope between rest and exercise > 3mmHg/L/min |
CO, cardiac output, CpcPH, combined post- and pre- capillary pulmonyary hypertension; PcpPH, isolated post-capillary pulmonary hypertension; mPAP, mean pulmonary arterial pressure; PAWP, pulmonary arterial wedge pressure; PH pulmonary hypertension; PVR, pulmonary vascular resistance; WU, Wood units. Some patients present with elevated mPAP (>20 mmHg) but low PVR (≤2 WU) and low PAWP (≤ 15 mmHg); this haemodynamic condition may be described by the term ‘unclassified PH’ (see text for further details.
Neben dem Kardinalsymptom, der Dyspnoe, und einem damit verbundenen Sauerstoffmangel ist die Symptomatik oft unspezifisch.1
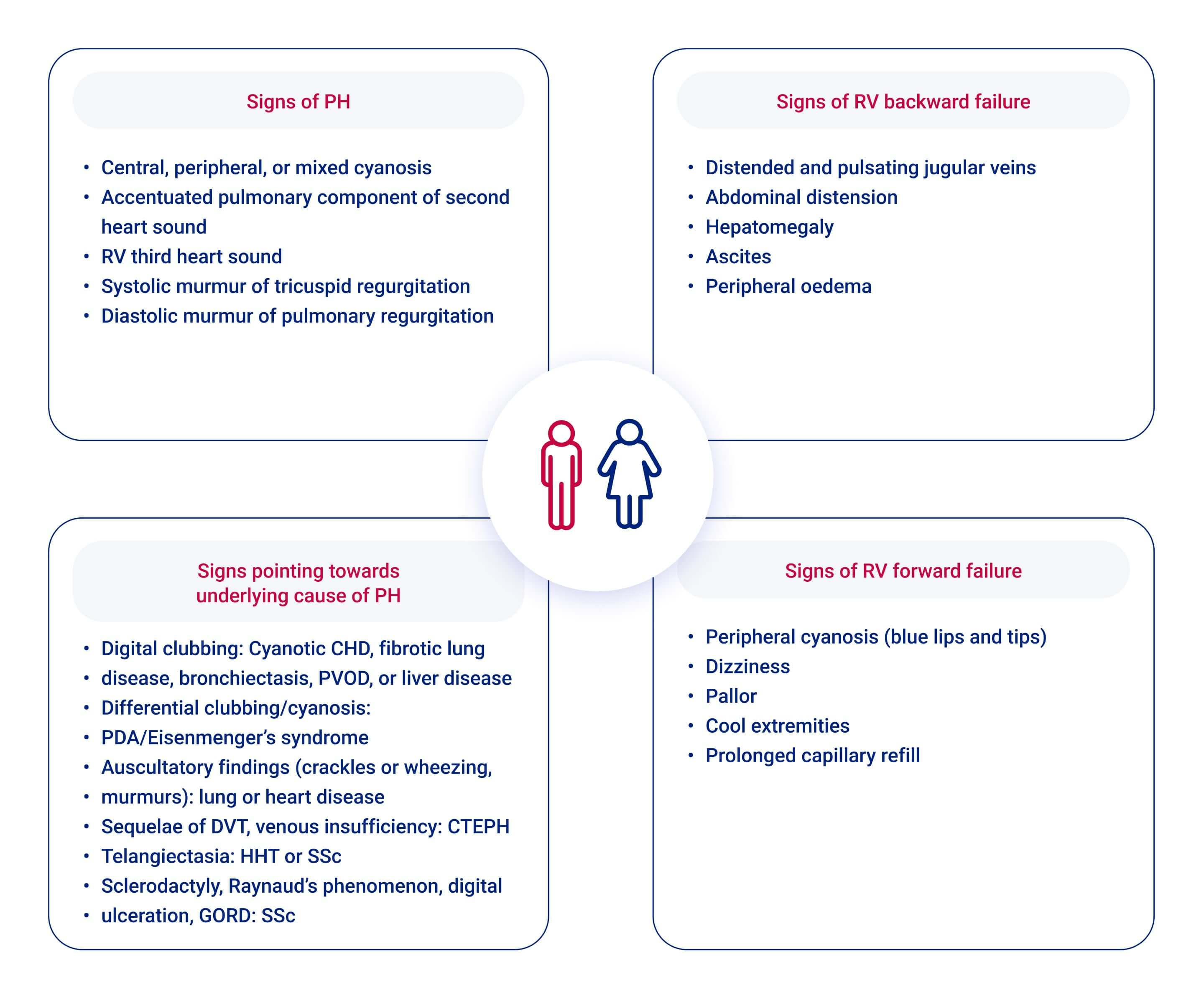
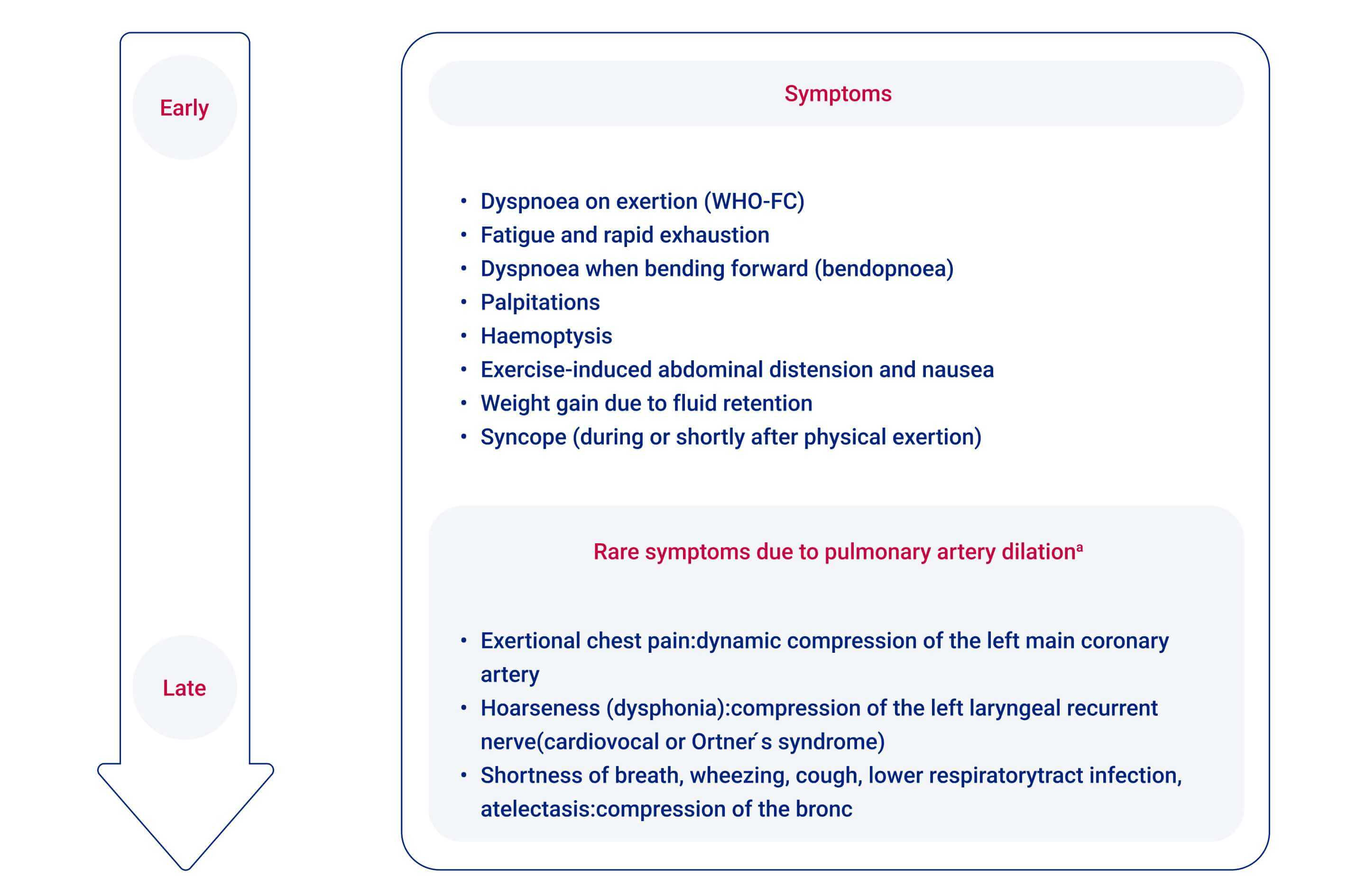
CHD, congenital heart disease; CTEPH, chronic thrombo-embolic pulmonary hypertension; DVT, deep venous thrombosis; GORD, gastro-oesophageal reflux disease; HHT, hereditary haemorrhagic telangiectasia; PDA, patent ductus arteriosus; PH, pulmonary hypertension; PVOD, pulmonary veno-occlusive disease; RV, right ventricle; SSc, systemic sclerosis; WHO-FC, World Health Organization functional class. aThoracic compression syndromes are found in a minority of patients with PAH with pronounced dilation of the pulmonary artery, and may occur at any disease stage and even in patients with otherwise mild functional impairment.
Die PH gilt als häufige, schwerwiegende und zugleich komplexe Erkrankung, welche als das gemeinsame Endstadium verschiedener Krankheitsprozesse (z. B. Linksherzerkrankungen, Lungenerkrankungen und -embolien) betrachtet werden kann.3
Etwa 1 % der globalen Bevölkerung ist an einer PH erkrankt, wobei die Prävalenz bei Personen über 65 Jahren erhöht ist.1 Je nach Unterform variieren die Inzidenzen.1 Während z. B. die Linksherzinsuffizienz als die häufigste Todesursache weltweit gilt und die Hälfte der Fälle davon zusätzlich von einer PH betroffen ist, stellt die PAH eine seltene, aber schwerwiegende Unterform der PH dar.1
Diagnostik der PH
Algorithmus zur Diagnostik bei Patientinnen und Patienten mit ungeklärter Dyspnoe und/oder Verdacht auf PH:
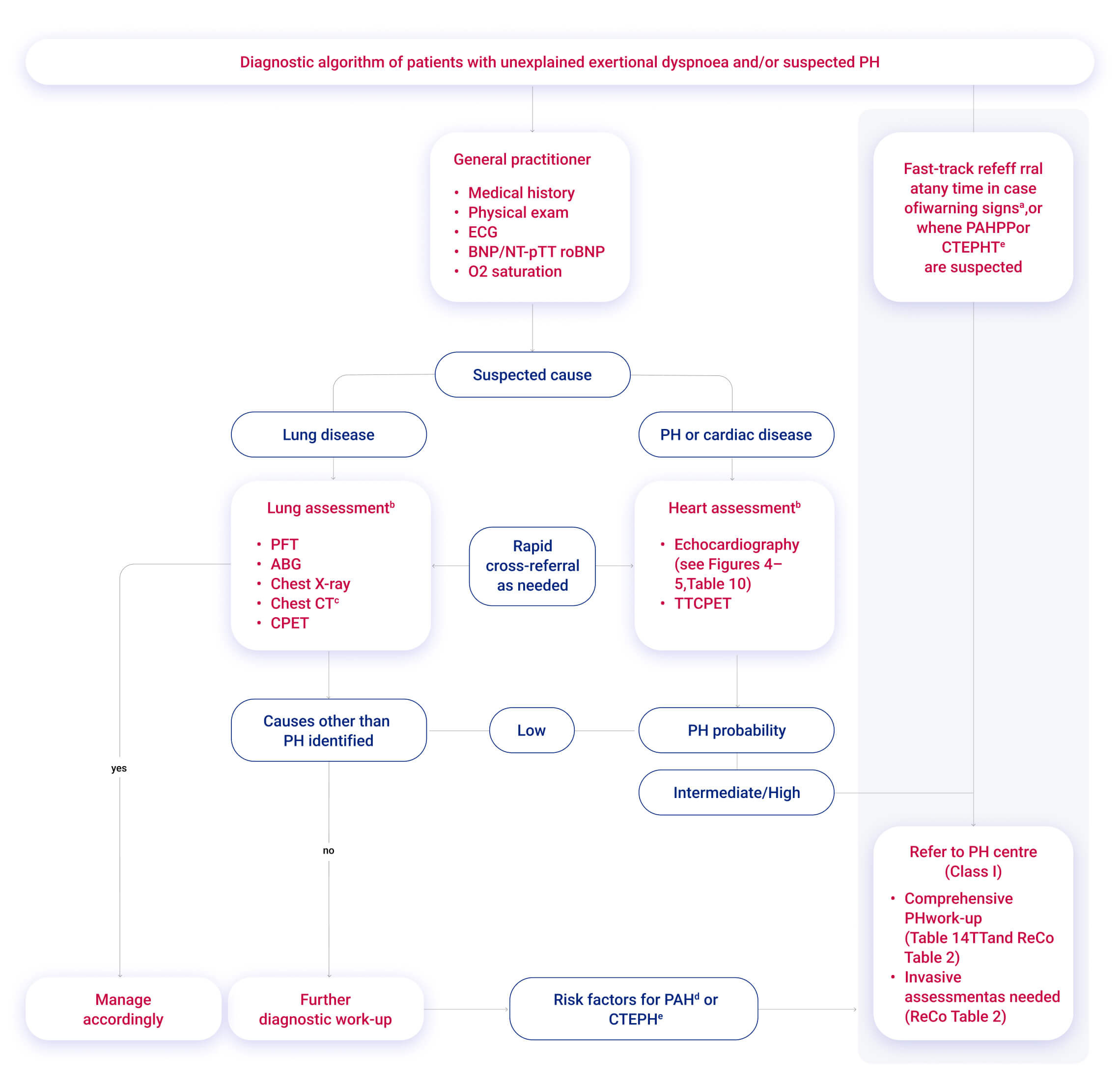
Warnzeichen, wie z.B. Dyspnoe, werden zunächst im niedergelassenen Bereich erkannt. Daraufhin sollten Differenzialdiagnostik, Klassifizierung und Therapiemanagement im PH-Expertenzentrum erfolgen.1
Elektrokardiogramm (EKG)11EKG kann auf eine PH hinweisen, wenn die folgenden typischen Zeichen vorliegen:
CAVE: Ein normales EKG schließt eine PH nicht aus (Sensitivität beträgt 55 %, Spezifität 70 %), und in Arterielle Blutgasanalyse1,11Kann Grunderkrankungen identifizieren und zeigt meist eine leichte bis moderate Hypoxämie. CAVE: Normalwerte schließen eine PAH nicht aus. Dahingegen ist das arterielle pCO2 bei PAH praktisch immer erniedrigt (Median, 32 mmHg). | Thorax-Röntgenaufnahme 11Ist bei 90 % der PAH-Erkrankten zum Zeitpunkt der Diagnose auffällig. Dabei sind u. a. folgende Zeichen besonders relevant:
CAVE: Der Schweregrad der PH korreliert nicht mit dem radiologischen Befund, und ein normales Röntgenbild schließt eine PH bzw. PAH nicht aus.
Lungenfunktionstests (PFT)1,11Dienen grundlegend dem Aufdecken von Komorbiditäten mit Bestimmung der Diffusionskapazität (DLCO). CAVE: Sogar bei schwerer PAH können normale Lungenfunktionswerte vorkommen. Bei einer PAH assoziiert mit CHD (PH-Gruppe 1) oder PH-Gruppe 3 sind schwere Abnormalitäten des PFT üblicher. Bei allen Unterformen ist eine geringe DLCO mit einer schlechten Prognose assoziiert. |
PH-ExpertenzentrumBestätigung der Diagnose mit Rechtsherzkatheter (RHC) und/oder Vasoreaktivitätstest insbesondere bei Verdacht auf PAH oder CTEPH.1 Unter anderem auch:1,11
| |
Diagnostische Parameter
Die wegweisenden Parameter der Diagnostikverfahren finden Sie hier:
Abweichungen im EKG können auf eine PH hinweisen.1
Auffälligkeiten im EKG bei PH-Erkrankten
Charakteristische Auffälligkeiten im EKG bei PH |
|---|
• P pulmonale (P > 0,25 mV in Ableitung II) • Rechts- oder Sagittalachsenabweichung (QRS-Achse > 90° oder unbestimmbar) • RV-Hypertrophie (R/S > 1, mit R > 0,5 mV in V1; R in V1+2 in Ableitung V5 >1 mV) • Rechtsschenkelblock — komplett oder inkomplett (qR oder rSR-Muster in V1) • RV-Belastunga (ST-Senkung/T-Welleninversion in den rechts präkordialen [V1–4] und inferioren [II, III, aVF] Ableitungen) • Verlängertes QTc-Intervall (unspezifisch)b |
EKG, Elektrokardiogramm; PH, pulmonale Hypertonie; Qtc, korrigiertes QT-Intervall; RV, rechtsventrikulär.
avorhanden bei fortgeschrittener PH.
bPH-Erkrankte können sich mit verlängertem QTc-Intervall (unspezifisch) präsentieren, das auf eine RV-Dysfunktion und verzögerte myokardiale Repolarisation deuten kann, und ein unabhängiger Prädiktor für die Mortalität ist.
Modifiziert nach 1.
Anzeichen einer LHD, PH und pulmonale Ödeme können detektiert werden.1
Radiografische Anzeichen einer PH und begleitende Anomalien
Anzeichen einer PH und begleitende Anomalien | Anzeichen einer LHD/ mit Lungenödem | Anzeichen einer Lungenerkrankung |
|---|---|---|
Rechtsherzhypertrophie | Zentrale Trübung des Luftraums | Abflachung des Diaphragmas (COPD/Emphysem) |
Pulmonalarterienhypertrophie (inklusive aneurysmatischer Dilatation) | Interlobuläre Septumverdickung „Kerley B“-Linien | Hypertransparenz (COPD/Emphysem) |
Reduzierung der peripheren Gefäße | Pleuraergüsse | Volumenverlust der Lunge (fibrotische Lungenerkrankung) |
„Wasserflaschen-Form" der Herzsillhouettea | Linksatriale Vergrößerung (inklusive gespreizter Carina tracheae), Linksventrikuläre Dilatation | Retikuläres Muster (fibrotische Lungenerkrankung) |
COPD, chronisch obstruktive Lungenerkrankung; PA, Pulmonalarterie; PH, pulmonale Hypertonie.
aKann bei Betroffenen mit PH mit fortgeschrittener rechtsventrikulärer Insuffizienz und moderatem Perikarderguss vorkommen.
Modifiziert nach 1.
Hämodynamische Messungen während der Rechtsherzkatheteruntersuchung
Messgrößen | Normwerte |
|---|---|
Rechtsatrialer Druck, Mittelwert (RAP) | 2–6 mmHg |
Pulmonal arterieller Druck, systolisch (sPAP) | 15–30 mmHg |
Pulmonal arterieller Druck, diastolisch (dPAP) | 4–12 mmHg |
Pulmonal arterieller Druck, Mittelwert (mPAP) | 8–20 mmHg |
Pulmonalarterienverschlussdruck, Mittelwert (PAWP) | ≤15 mmHg |
Herzzeitvolumen (CO) | 4–8 L/min |
Gemischte venöse Sauerstoffsättigung (SvO2)a | 65–80% |
Arterielle Sauerstoffsättigung (SaO2) | 95–100% |
Systemischer Blutdruck | 120/80 mmHg |
Berechnungsparameter | |
Pulmonalvaskulärer Widerstand (PVR)b | 0,3–2,0 WU |
Pulmonalvaskulärer Widerstandsindex (PVRI) | 3–3,5 WU·m2 |
Totaler pulmonaler Widerstand (TPR)c | <3 WU |
Herzindex (CI) | 2,5–4,0 L/min·m2 |
Schlagvolumen (SV) | 60–100 mL |
Schlagvolumenindex (SVI) | 33–47 mL/m2 |
Pulmonalarterielle Compliance (PAC)d | >2,3 mL/mmHg |
WU, Wood-Einheiten. aAbgeleitet aus einer Blutprobe aus der Pulmonalarterie; Kompartiment-Oximetrie zum Ausschluss eines intrakardialen Shunts ist empfohlen, wenn SvO2 >75%. bPVR, (mPAP−PAWP)/CO. cTPR, mPAP/CO. dPAC, SV/(sPAP−dPAP).
Modifiziert nach 1.
Applikationsweg, Halbwertszeit, Dosierungen und Anwendungsdauer der empfohlenen Prüfsubstanzen zur Vasoreaktivitätstestung bei pulmonaler arterieller Hypertonie
Substanz | Halbwertszeit | Dosierung | Anwendungsdauer |
|---|---|---|---|
Stickstoffmonoxid129, inh | 15–30 s | 10–20 ppm | 5–10 mina |
Iloprost130,131, inh | 30 min | 5–10 μgb | 10–15 minc |
Epoprostenol129, i.v. | 3 min | 2–12 ng/kg/min | 10 mind |
inh, inhalativ; i.v., intravenös.
aMessung als Einzelschritt innerhalb des Dosisbereichs. bAm Mundstück. cMessung als Einzelschritt; volle Wirkung ist zeitlich begrenzt. dInkrementelle Steigerung in 2 ng/kg/min-Intervallen, Dauer zehn Minuten bei jedem Schritt.
Modifiziert nach 1.
Rolle der Expertenzentren
PH-Expertenzentren führen die Differenzialdiagnostik und die darauffolgende klinische Klassifizierung der PH leitlinienkonform durch.1,11
Anforderungen:1,11
Spezialisierte Fachärzte, i. d. R. aus dem Bereich der Pneumologie und/oder Kardiologie
Invasive Methoden im klinischen Kontext
Ambulante und stationäre Betreuung inklusive Intensivversorgung durch PH-Experten rund um die Uhr
Spezialisierte Pflegekräfte und Fachkräfte für psychologische und soziale Betreuung
Kooperation u. a. mit Zentren für angeborene Herzfehler oder genetische Untersuchungen, Lungentransplantationsprogramm und Selbsthilfeorganisationen
Erfahrung mit für die PAH zugelassenen Medikamenten und Teilnahme an klinischen Phase-II/III-Studien sowie epidemiologischen Krankheitsregistern
Übersicht der Aufgaben von PH-Expertenzentren gemäß ECS/ESR-Guideline1

Modifiziert nach 1.
Anforderungen nach G-BA
Die Versorgung der PH-Patientinnen und -Patienten erfolgt durch ein interdisziplinäres Team gemäß § 3 Richtlinie ambulant spezialfachärztliche Versorgung (ASV-RL).12
Teamleitung und Kernteam aus den Fachbereichen:12
Innere Medizin und Kardiologie oder
Innere Medizin und Pneumologie
Beratende Fachärztinnen und -ärzte (bei Bedarf):12
Humangenetik
Innere Medizin und Gastroenterologie
Innere Medizin und Rheumatologie
Laboratoriumsmedizin
Nuklearmedizin
Psychiatrie und Psychotherapie oder psychosomatische Medizin und Psychotherapie oder
Psychologische oder ärztliche Psychotherapie
Radiologie
Enge Zusammenarbeit mit folgenden Gesundheitsfachdisziplinen und weiteren Einrichtungen:12
Transplantationszentren (Lunge, Herz)
sozialen Diensten wie z. B. Sozialdienst oder vergleichbaren Einrichtungen mit sozialen Beratungsangeboten
Physiotherapie
Anforderungskatalog:12
24-Stunden-Notfallversorgung mindestens in Form einer Rufbereitschaft
Intensivmedizinischen Behandlung möglich
Vorhandensein von Notfallplänen (SOP) und für Reanimation und sonstige Notfälle benötigten Geräten und Medikamenten
Dokumentation der Diagnostik und Behandlung zur Diagnosesicherheit
Kernteam muss mindestens 50 PH-Patientinnen und -Patienten mit Verdachts- oder gesicherter Diagnose behandeln
Es besteht ein Überweisungserfordernis durch die behandelnde Vertragsärztin oder den behandelnden Vertragsarzt (auch mit einer Verdachtsdiagnose möglich).
Leistungen zu Diagnostik und Therapie:12
Allgemeine Herzfunktionsdiagnostik (z. B. EKG) und spezielle Herzfunktionsdiagnostik (z. B. transösophageale [TEE] und transthorakale [TTE] Echokardiographie, Belastungs-EKG, Rechtsherzkatheter [gegebenenfalls mit pharmakologischer Testung])
Bildgebende Diagnostik (z. B. Röntgenuntersuchung, Sonographie, Doppleruntersuchung, Ventilations-Perfusions-Szintigraphie, CT, MRT, Pulmonalarterienangiographie, Myokardszintigraphie)
Endoskopie des oberen Gastrointestinaltraktes
Endoskopie des Respirationstraktes
Humangenetische Untersuchungen (z. B. BMPR2, ALK1)
Körperliche Untersuchung
Laboruntersuchungen (z. B. Blutgasanalyse)
Lungenfunktionsmessungen (z. B. Diffusionskapazitätsanalyse der Lunge für
Kohlenmonoxid [DLCO]
Polygraphie und Polysomnographie im Rahmen der Differenzialdiagnostik und Therapie der schlafbezogenen Atmungsstörungen
Spiroergometrie
Ausstellen z. B. von Bescheinigungen, Anträgen, Berichten
Behandlungsplanung, -durchführung und -kontrolle
Behandlung von Therapienebenwirkungen, Komplikationen und akuten unerwünschten Behandlungsfolgen
Behandlung in Notfallsituationen
Einleitung der Rehabilitation
Medikamentöse Therapien inklusive Inhalations- und Infusionstherapie
Physikalische Therapie
Psychotherapeutische Beratung und Betreuung
Therapeutische Punktionen und Drainagen
Diagnostik und Behandlung
Hilfsmitteln inklusive Anleitung zum Gebrauch
humangenetischen Fragestellungen
Medikamentengabe und Nebenwirkungen
psychosozialen Beratungs- und Betreuungsangeboten
Rehabilitationsangeboten
sozialen Beratungsangeboten
Verhalten in Notfallsituationen. Die Information kann z. B. mittels eines Notfallausweises erfolgen.
vorhandenen Selbsthilfeangeboten
Gründe für die Überweisung an ein PH-Expertenzentrum
Klinische Befunde
Ergibt sich bei der klinischen Untersuchung einer Patientin oder eines Patienten eine RV-Dysfunktion bei der Echokardiographie, erhöhte Werte kardialer Biomarker und/oder eine hämodynamische Instabilität, sollte sofort an ein PH-Expertenzentrum überwiesen werden.1
Risikofaktoren und besondere Situationen
Bei Verdacht auf PH ist eine Überweisung an das PH-Expertenzentrum zur Abklärung der Differenzialdiagnose nötig, wenn:1
Eine Intermediäre/hohe Wahrscheinlichkeit einer PH vorhanden ist, oder
Risikofaktoren für eine PAH bestehen, oder
in der Vergangenheit Lungenembolien aufgetreten sind, oder
besondere Umstände wie Schwangerschaft, Operationen oder Flugreisen bei Risikopatientinnen/-patienten vorliegen oder anstehen.
Weitere Warnzeichen
Mögliche Warnzeichen zu jeder Zeit:1
schwerwiegende, progrediente Symptome
Synkope(n)
schlecht tolerierte Arrhythmien
beeinträchtigter/verschlechterter hämodynamischer Zustand (Hypotonie, Tachykardie)
Verdacht auf PH?
Bei Verdacht auf PH nutzen Sie unseren Expertenfinder und kontaktieren Sie unsere PH-Experten hier auf der Plattform oder ein PH-Expertenzentrum in Ihrer Nähe.

COPD: Chronisch obstruktive Lungenerkrankung
CpcPH: Kombinierte post- und präkapilläre pulmonale Hypertonie
CPET: Leistungsdiagnostik/Ergospirometrie
CTEPH: Pulmonale Hypertonie aufgrund chronischer Thromboembolien
EKG: Elektrokardiogramm
G-BA: Gemeinsamer Bundesausschuss
IpcPH: Isolierte postkapilläre pulmonale Hypertonie
LHD: Linksherzerkrankung
mPAP: Mittlerer Pulmonalarteriendruck
PAH: Pulmonale arterielle Hypertonie
PAWP: Pulmonalarterienverschlussdruck
PFT: Lungenfunktionstest
PH: Pulmonale Hypertonie
PVR: Pulmonalvaskulärer Widerstand
RHC: Rechtsherzkatheteruntersuchung
RV-Dysfunktion: Rechtsventrikuläre Dysfunktion
WHO: World Health Organization
Humbert M et al. Eur Heart J 2022; 43(38): 3818–3731.
Rosenkranz S. Dtsch Med Wochenschr 2013; 138(37): 1820.
DGPK, S2k-Leitlinie Pulmonale Hypertonie, Version 3.0, Stand 29.04.2020; verfügbar unter: https://register.awmf.org/de/leitlinien/detail/023-038 (letzter Zugriff am 08.04.2024).
Deaño RC et al. JAMA Intern Med 2013; 173(10): 887–893.
Rich S et al. Ann Intern Med 1987; 107(2): 216–223.
Humbert M et al. Am J Respir Crit Care Med 2006; 173(9): 1023–1030.
Brown LM et al. Chest 2011; 140(1): 19–26.
Badesch DB et al. Chest 2010; 137(2): 376–387.
Didden EM et al. Pulm Circ 2023; 13(1): e12188.
Held M et al. Dtsch Med Wochenschr 2014; 139(33): 1647–1652.
Hoeper MM et al, Diagnostik und Therapie der pulmonalen Hypertonie, Europäische Leitlinien 2009, verfügbar unter: https://leitlinien.dgk.org/files/2010_Leitlinie_pulmonale_Hypertonie.pdf (letzter Zugriff am 08.04.2024).
G-BA, Richtlinie des Gemeinsamen Bundesausschusses über die ambulante spezialfachärztliche Versorgung nach § 116b SGB V, verfügbar unter: https://www.g-ba.de/downloads/62-492-3390/ASV-RL_2023-06-15_iK_2024-03-01.pdf (letzter Zugriff am 08.04.2024).